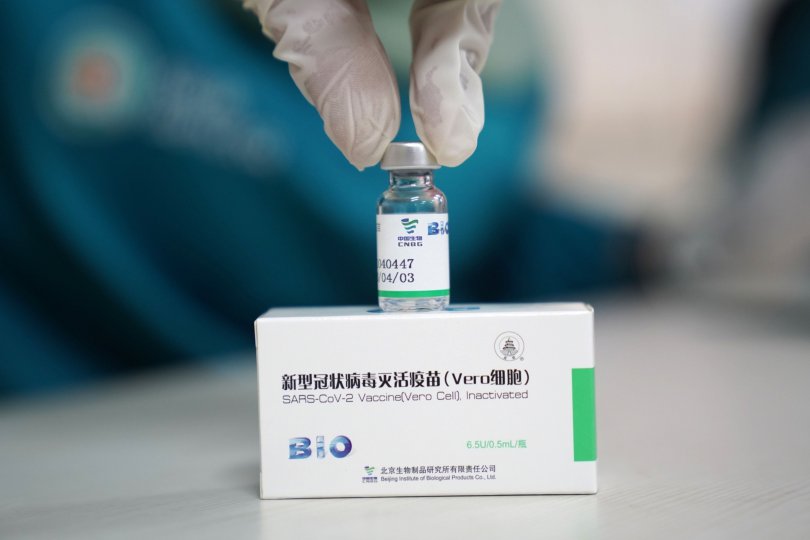
ხანგრძლივი მოლოდინის შემდეგ, ჩინური Sinopharm-ის Covid-19-ის ვაქცინის კვლევის ბოლო ეტაპის დეტალური მონაცემები სამედიცინო ჟურნალში პირველად გამოქვეყნდა.
ამერიკის სამედიცინო ასოციაციის ჟურნალში (JAMA) გუშინ გამოქვეყნებული მონაცემების თანახმად, China National Biotec Group-ის მიერ შემუშავებული ორი ინაქტივირებული ვაქცინა, სიმპტომური ინფექციების 72.8%-იან და 78.1%-იან პრევენციას უზრუნველყოფს, რაც შეესაბამება იმ მონაცემებს, რასაც კომპანია ამ დრომდე აცხადებდა.
JAMA-ში გამოქვეყნებულ კვლევაში ჩართული იყო 40 832 მოხალისე არაბთა გაერთიანებული საამიროებიდან, ბაჰრეინიდან, ეგვიპტიდან და იორდანიიდან. კვლევის მონაწილეები სამ თანაბარ ჯგუფად გაყვეს და სამი კვირის ინტერვალით გაუკეთეს ორი ვაქცინის (WIV04 და HBO2 დასახელებით) ორი დოზა ან პლაცებო. მეორე დოზის გაკეთებიდან ორ კვირაში, ერთ ჯგუფში ინფექცია 26, მეორე ჯგუფში 21 პირს შეხვდა. იმ ჯგუფიდან, სადაც ვაქცინის ნაცვლად, პლაცებო მიიღეს, ვირუსით 95 ადამიანი დაინფიცირდა.
ვაქცინით აცრილმა მოხალისეებმა Covid-19 გართულების გარეშე გადაიტანეს, მაშინ, როცა ორ პირს, ვისაც პლაცებო ჰქონდა მიღებული, მდგომარეობა გაუმწვავდა.
ასე რომ, კვლევაში ქალებში, მოხუცებსა და ჯანმრთელობის პრობლემის მქონე პირებში ვაქცინის ეფექტიანობისა და უსაფრთხოების შესახებ მონაცემები მწირია.
China National Biotec Group-ის განცხადებაში აღნიშნულია, რომ კვლევა ჟურნალს 17 მარტს გადაეგზავნა, თუმცა გამოქვეყნების დასტური 12 მაისს მიიღო.
გამოქვეყნებული კვლევა გარკვეულ შეზღუდვებზე მიუთითებს. კერძოდ, მონაწილეთა 85%-ს მამაკაცები შეადგენდნენ. 60+ ასაკის მოხალისეები კი საერთო რაოდენობის 2%-ს წარმოადგენდნენ და ასევე, მონაწილეების უმრავლესობა ჯანმრთელი იყო.
ჩინური ვაქცინების მწარმოებლებს, მათ შორის, Sinopharm-ს ხშირად აკრიტიკებენ იმის გამო, ისინი პროდუქტის უსაფრთხოებისა და ეფექტიანობის შესახებ მონაცემებს ადეკვატურად არ აქვეყნებენ. გაუმჭვირვალობამ ვაქცინის ეფექტიანობასთან დაკავშირებით კითხვები არაერთ ქვეყანაში გააჩინა. ეჭვები კიდევ უფრო გააძლიერა "ჯანდაცვის მსოფლიო ორგანიზაციის" (WHO) მიერ დამტკიცების დაგვიანებამ ჩილესა და სეიშელის კუნძულებზე გამოკვეთილმა ტენდენციამ. მიუხედავად იმისა, რომ ამ ქვეყნებში მოსახლეობის მნიშვნელოვანი ნაწილი Sinopharm-ის ვაქცინით იყო აცრილი, ორივეგან ინფიცირების შემთხვევებმა მნიშვნელოვანად მოიმატა.
"ჯანმრთელობის მსოფლიო ორგანიზაციამ" Sinopharm-ის ერთ ვაქცინას, რომელიც პეკინის ბიოლოგიური პროდუქტების ინსტიტუტის მიერაა წარმოებული, ავტორიზაცია 7 მაისს მიანიჭა. ამ ვაქცინით 18+ მოქალაქეების აცრა საქართველოში 7 მაისს დაიწყო.
Bloomberg-ის ორიგინალური სტატია